Сущность процессов горения и взрывов
В наиболее общей формулировке горение представляет собой быстро протекающую физико-химическую реакцию с выделением тепла и света. В природе и в технике чаще всего наблюдаются процессы горения, связанные с окислением горючих веществ кислородом воздуха. Однако многие вещества вступают между собой в реакцию горения и при отсутствии кислорода. Так, водород и некоторые металлы горят в газообразном хлоре, медь — в парах серы, алюминий в броме и т. п.
Наряду с реакциями горения, протекающими в результате химического соединения различных веществ, происходят реакции горения, связанные с разложением газов, жидкостей и твердых веществ (ацетилен, нитроглицерин, нитроклетчатка, азид свинца и др.).
Разновидностью горения является взрыв и детонация, когда реакция соединения или разложения веществ протекает со скоростью сотен и даже тысяч метров в секунду.
Различают твердые, жидкие и газообразные (парообразные) горючие вещества. Твердые и жидкие вещества могут находиться в воздухе во взвешенном состоянии (в виде пыли или тумана).
Горение возможно лишь при определенных условиях: наличие горючего вещества и вещества, поддерживающего процесс горения, и достаточный их нагрев. Начавшееся горение может продолжаться только при условии, если количество тепла, выделяющегося при горении, превышает теплоотдачу в окружающую среду. К горению относят также взрыв и детонацию.
Продуктами горения при полном сгорании веществ являются негорючие газы и вода. При неполном сгорании в продуктах горения содержатся окись углерода и другие горючие соединения.
Следует отметить, что тяжелые несчастные случаи при пожарах нередко происходят из-за чрезмерной задымленности и наличия окиси углерода в зоне пожара.
В процессе горения выделяется большое количество тепла, которое определяется теплотой сгорания горючих веществ. Отдача тепла в окружающую среду во время пожара происходит конвекцией и главным образом излучением. Температура горения зависит в основном от теплоты сгорания горючих веществ и от количества образующихся продуктов горения.
Горючие вещества могут воспламеняться при непосредственном контакте с высоконагретыми телами или с открытым пламенем, при нагревании излучением, а также при протекании в горючем веществе экзотермических реакций.
Окислительный процесс горения включает фазы предварительного нагрева, окисления, самовоспламенения и последующего горения. На рисунке 1 приведена кривая изменения температур процесса горения во времени. При нагревании горючего вещества с начальной температурой tн до темпратуры начала окисления tо наблюдается медленное повышение температуры, поскольку подводимое извне тепло расходуется на плавление, испарение или разложение горючих веществ. После нагрева горючего вещества до tо нарастание температуры горения во времени происходит быстрее в связи с выделением тепла при начавшейся реакции окисления.
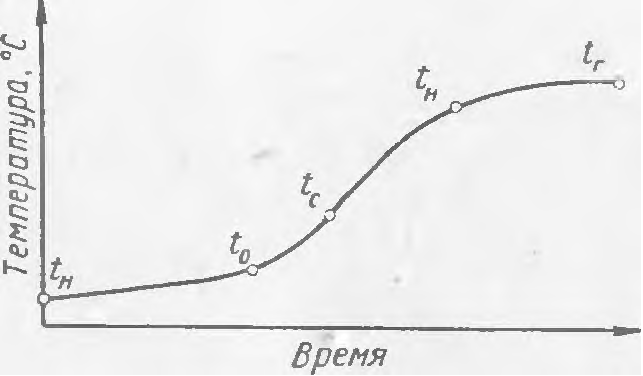
Однако температура tо еще недостаточна для дальнейшего саморазогревания, так как теплоотдача в окружающую среду превышает образование тепла при начавшейся реакции окисления. По достижении температуры самовоспламенения tc наступает равновесие между приходом тепла к горючему веществу и теплоотдачей в окружающую среду. В результате происходит дальнейший быстрый подъем температуры. При температуре tп появляется пламя и начинается устойчивый процесс горения tг.
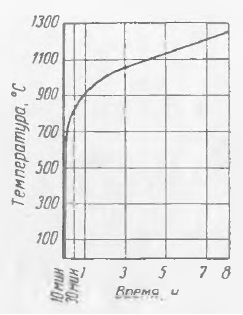
Кривая зависимости температуры от времени при пожаре приведена на рисунке 2.
Горение является весьма сложным физико-химическим процессом. По современным представлениям, в процессе горения возникают малоустойчивые, но весьма активные промежуточные продукты в виде свободных атомов, перекисей, радикалов. Реакционная способность кислорода значительно увеличивается при нагревании.
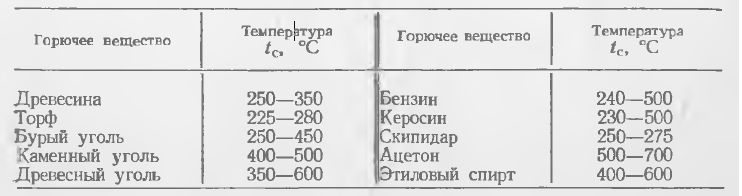
Температура самовоспламенения горючих веществ колеблется в широких пределах не только для различных веществ, но и для одного и того же вещества. Эта температура зависит от многих переменных факторов: концентрации смеси, давления, объема сосуда (для газо- паро- и пылевоздушных смесей), измельченное™ (для твердых горючих веществ). В таблице 1 приведены пределы колебания температуры самовоспламенения некоторых горючих веществ.
Взрывы смесей горючих газов, паров и пыли с воздухом могут происходить только при условии предварительного смешивания их горючих составляющих с кислородом воздуха. Для различных газов, паров и пыли существуют определенные границы взрывоопасных концентраций, являющиеся нижним и верхним пределами взрывоопасной смеси. При содержании горючих составляющих в смеси менее нижнего предела смесь не взрывается и не горит, а при содержании горючих веществ более верхнего предела смесь не взрывается, но горит и, следовательно, является пожароопасной.
Чем меньше нижний предел взрывной концентрации, тем опаснее горючее вещество. Взрывоопасность смесей определяется также интервалом между нижним и верхним пределами смеси. Чем больше этот интервал, тем опаснее взрывная смесь. Так, у ацетилена (С2Н2) нижний предел взрываемости смеси с воздухом (в объемных процентах) равен 2,6%, а верхний 82%. У метана (СН4) эти значения соответственно составляют 5,3 и 14%. Следовательно, взрывоопасность ацетилена значительно больше взрывоопасности метана.
Температура при взрыве смесей газов и паров колеблется в широких пределах и составляет 1500—3000 °С, а развиваемое при взрыве давление обычно не превышает 1,1 мн/м2 (11 атм). Однако при увеличении содержания кислорода в смеси и при сжатии смеси во время взрыва (например, в газопроводах -большой длины) давление взрыва может сильно возрасти и даже перейти в детонацию, когда скорость распространения пламени достигает 1000—4000 м/сек, а давление составляет 8 Мн/м2 (80 атм) и более.
Пожарная опасность твердых горючих веществ
Пожарная опасность твердых веществ определяется их составом и в значительной степени зависит от удельной поверхности этих веществ. Так, бумага в рулонах горит очень медленно, между тем как горение развернутой бумаги происходит весьма быстро. .При повышении влажности твердых веществ значительно уменьшается их воспламеняемость и скорость горения. Скорость горения твердых веществ зависит также от количества летучих продуктов, выделяющихся при разложении веществ во время горения; с увеличением летучих составляющих возрастает и скорость горения.
При горении твердых веществ наблюдаются процессы пламенного и беспламенного горения. При беспламенном горении окисление горючего вещества происходит в поверхностном слое. Одним из основных горючих газов при гашении веществ, содержащих углерод, является окись углерода.
Щелочные металлы начинают гореть после их расплавления (некоторые из них образуют пламя при взаимодействии с водой). Горение алюминия, магния и кальция сопровождается образованием значительного количества белого дыма, состоящего из окислов этих металлов. Процесс горения щелочных металлов значительно интенсифицируется при их измельчении. Так, стружка магния и магниевых сплавов (например, электрон) горит весьма интенсивно. Пыль этих металлов в состоянии аэрогеля (в виде отложений) горит медленно, однако, будучи приведена во взвешенное состояние, она взрывается.
Горение древесины — сложный процесс. При повышении температуры древесины до 110—130 °С выделяется вода, а затем начинается разложение древесины. Продукты разложения в пределах 130—200 °С состоят из паров воды и углекислого газа. При дальнейшем повышении температуры в составе выделяющихся газов появляется окись углерода, водород, метан и другие горючие газы. При 230—250 °С продукты разложения древесины воспламеняются от постороннего источника тепла, после чего древесина продолжает гореть. При 300 °С из древесины выделяется максимальное количество горючих газов.
Фаза пламенного горения древесины постепенно, по мере образования на ее поверхности слоя угля, уменьшается и наступает фаза беспламенного горения этого угля. После выгорания слоя угля вновь интенсивно выделяются горючие газы и появляется пламя. Затем образуется новый слой угля и наступает фаза беспламенного горения и т. д.
По окончании ряда циклов пламенного и беспламенного горения, когда вся древесина разложилась, происходит горение остатков древесного угля без выделения пламени.
Следует отметить, что при длительном нагревании древесины в последней возникают процессы разложения и окисления, что может снизить температуру воспламенения древесины до 110—130 °С.
Пожарная опасность жидких горючих веществ
Пожарная опасность горючих жидкостей определяется температурой вспышки паров испаряющейся жидкости при (внесении источника тепла. Температура вспышки представляет собой наименьшую температуру, при которой пары горючего вещества создают над его поверхностью паровоздушную смесь, воспламеняющуюся при внесении источника тепла (например, открытого огня).
За время вспышки поверхность горючей жидкости не прогревается до температуры, достаточной для интенсивного испарения жидкости, и дальнейшее горение прекращается. Если температура жидкости в момент вспышки окажется достаточной для того, чтобы вслед за вспышкой последовало горение, то такую температуру называют температурой воспламенения горючей жидкости.
Чем ниже температура вспышки горючей жидкости, тем больше пожарная опасность По существующей классификации все горючие жидкости разделяются на два класса. К I классу относятся жидкости с температурой вспышки менее 45°С (например, бензин, спирт, эфир, керосин и др.), а ко II классу—жидкости с температурой вспышки более 450С (например, масла, мазуты и др.). Огнеопасные жидкости I класса относят к легковоспламеняющимся жидкостям, а жидкости II класса — к горючим.
Следует отметить, что пожарная опасность ряда твердых веществ (например, нафталин, фосфор, камфора и др., которые испаряются при нормальной температуре) также характеризуется температурой вспышки.
У легковоспламеняющихся жидкостей небольшая (1—2°С) разница между температурой вспышки паров и температурой воспламенения. У горючих жидкостей эта разница достигает 30 0С и более.
Пожарная опасность жидкостей увеличивается с понижением температуры вспышки, температуры воспламенения и самовоспламенения, а также с увеличением скорости испарения и уменьшением нижнего предела концентрации взрывоопасной смеси паров жидкости с воздухом.
Пожарная опасность пыли
Пыль горючих веществ в состоянии аэрогеля (в виде отложений пыли) может тлеть и гореть, а находясь в форме аэрозоля, т. е. будучи взвешенной в воздухе, она способна взрываться, образуя взрывоопасные пылевоздушные смеси. Горению пыли в значительной мере способствует адсорбция пылью кислорода воздуха. Взрывоопасность пыли повышается с уменьшением частиц пыли вследствие увеличения ее удельной поверхности. Температура самовоспламенения горючей пыли обычно колеблется в пределах 700—900°С, но некоторые виды пыли имеют относительно низкую температуру самовоспламенения (например, сажа взрывается при 360 °С).
Аналогично горючим газам и парам у пыли существует нижний и верхний пределы взрывоопасной концентрации. Нижний предел взрывной концентрации (источник тепла — раскаленное тело) для серной пыли составляет 7, сахарной 10,3, алюминиевой 7 и каменноугольной 17,2 г/м3.
Пределы взрывоопасной концентрации пыли зависят от влажности, дисперсности, температуры и мощности источника тепла и других факторов. Развиваемое при взрывах пыли давление обычно не превышает 0,4—0,6 мн/м2 (4—6 атм).
Самовозгорание
Некоторые вещества обладают способностью адсорбировать газы и кислород воздуха, вследствие чего увеличивается скорость окислительных реакций и повышается температура этих веществ. Если при этом создаются условия, когда приход тепла будет больше отдачи в окружающую среду, то в результате непрерывного повышения температуры такие вещества могут гореть. Процесс, при котором горение (веществ происходит в результате самонагревания, называется самовозгоранием. Ясно, что вещества, у которых процесс самовозгорания начинается при низкой температуре, представляют повышенную пожарную опасность.
Вещества, способные к самовозгоранию, разделяют на несколько групп. К I группе относятся вещества растительного происхождения, например влажное зерно, сено, опилки. Причиной повышения температуры для них являются биологические процессы; в дальнейшем повышение температуры происходит вследствие окисления, что приводит к самовозгоранию таких веществ.
Ко II группе относят каменные и бурые углы (кроме тощих углей) и торф. Самовозгоранию торфа способствуют протекающие в нем биологические процессы. Торф самовозгорается при относительно невысокой температуре (120- 140°С).
К III группе относятся масла и жиры, причем повышенную пожарную опасность представляют масла растительного происхождения (льняное масло и др.), так как они содержат непредельные органические соединения, которые могут окисляться и полимеризоваться. Животные и минеральные масла представляют значительно меньшую пожарную опасность.
Опасность самовозгорания резко возрастает в тех случаях, когда масла попадают на обтирочные материалы и на спецодежду. Образующаяся на поверхности этих материалов пленка масла адсорбирует кислород воздуха, вследствие чего происходит повышение температуры, возможно воспламенение материалов. В практике металлургических заводов известны случаи пожаров из-за самовозгорания замасленных обтирочных материалов и спецодежды.
К IV группе относятся химические вещества и некоторые соединения. К этой группе относятся вещества, способные к самовозгоранию при их контакте с воздухом, например фосфористый водород, кремниевый водород, белый фосфор, арсины, пыль алюминия и цинка, свежеприготовленные древесный уголь и сажа, металлоорганические соединения. Сульфиды железа FeS и Fe2S3 обладают пирофорными свойствами. При соприкосновении этих сульфидов с воздухом температура их повышается настолько высоко, что является источником воспламенения горючих веществ.
Ряд веществ воспламеняется при соприкосновении с водой, например щелочные металлы, карбиды кальция и щелочных металлов и др. Воспламенение возникает от того, что в результате взаимодействия этих веществ с водой образуются горючие газы, которые воспламеняются вследствие экзотермичности реакций. В сжатом кислороде самовозгораются масла и жиры.