В шихте содержатся некоторые количества окислов и более сложных соединений марганца, кремния, фосфора и в отдельных случаях легирующих и цветных металлов (хрома, ванадия, никеля и др.).
Ввиду различной термодинамической прочности окислов и соединений по ходу доменного процесса они восстанавливаются при различных условиях и с различной полнотой. Определенное влияние при этом оказывает химический характер окислов (основной или кислотный), определяющий их активность в соединениях и шлаке, а также химическое сродство восстанавливаемого элемента к железу и углероду, находящимся в чугуне. Некоторые вносимые в печь окислы (Al2O3, CaO, MgO) являются настолько химически прочными, что практически не подвергаются восстановлению — полностью переходят в шлак.
Восстановление марганца
В шихтовых материалах марганец находится в виде окислов MnO2, Mn2O3 (руды) или окислов Mn3O4, MnО и более сложных соединений (агломераты). Начальные стадии восстановления высших окислов протекают легко при минимальных содержаниях СО в газовой фазе. Упругость диссоциации для MnO2 и Mn2O3 достигает 101,325 кн/м2 (1 aт) при 565 и 1090° С соответственно. Перекись марганца MnO2 энергично восстанавливается до Mn2O3 и частично до Mn3O4 на верхних горизонтах засыпи при 300—400° С с выделением тепла. Восстановление Mn2O3 и Mn3O4 происходит в шахте печи при 400—800° С. При использовании марганцовистого агломерата высшие окислы Mn восстанавливаются при агломерации.
Однако закись марганца MnО весьма трудно восстановима. Ее восстановление происходит лишь с участием углерода и с затратой тепла, вдвое большей, чем при восстановлении FeO. Термодинамически осуществление этого процесса в стандартных условиях (аMnO= аMn = аC = 1, рCO = 1 aт) становится возможным, начиная с 1430° С.
В доменной печи MnО восстанавливается в несколько других условиях. При восстановленном металлическом железе и избытке углерода восстанавливаемый марганец переходит в металлический раствор (чугун), где может быть частично связан с углеродом в виде карбида. Таким образом, его термодинамическая активность, особенно в начале процесса восстановления, значительно меньше единицы. Это обстоятельство обеспечивает восстановление марганца углеродом при более низких температурах, чем 1430° С.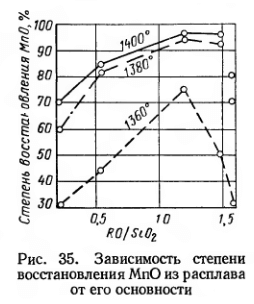 Однако восстановление марганца затрудняет образование соединений MnО с SiO2 (силикатов) и переход невосстановленной закиси марганца в доменный шлак. Исследования доменного процесса показывают, что большая часть МnО не успевает восстанавливаться до начала процесса шлакообразования и оказывается в составе шлаковой фазы. Образование силиката марганца из смеси его составляющих протекает очень интенсивно, начиная с 1100° С. По данным лабораторных исследований, восстановление марганца из закиси в смеси с активным древесным углем при 1300° С за час протекает на 34—38%, в то время как восстановление его из силиката при тех же условиях протекает лишь на 4,2%. Наличие извести в контакте с силикатами марганца значительно облегчает и ускоряет восстановление марганца. Для указанных выше условий степень восстановления марганца составила около 17%. При этом протекают следующие реакции:
Однако восстановление марганца затрудняет образование соединений MnО с SiO2 (силикатов) и переход невосстановленной закиси марганца в доменный шлак. Исследования доменного процесса показывают, что большая часть МnО не успевает восстанавливаться до начала процесса шлакообразования и оказывается в составе шлаковой фазы. Образование силиката марганца из смеси его составляющих протекает очень интенсивно, начиная с 1100° С. По данным лабораторных исследований, восстановление марганца из закиси в смеси с активным древесным углем при 1300° С за час протекает на 34—38%, в то время как восстановление его из силиката при тех же условиях протекает лишь на 4,2%. Наличие извести в контакте с силикатами марганца значительно облегчает и ускоряет восстановление марганца. Для указанных выше условий степень восстановления марганца составила около 17%. При этом протекают следующие реакции:
вытеснение MnО из силиката
MnО·SiO2 + 2СаО = 2СаО·SiO2 + MnО +110 кдж/моль (26,24 ккал/моль)
восстановление MnО углеродом
MnО + С = Mn + СО—288,8 кдж/моль (—68,93 ккал1моль);
суммарная реакция MnO·SiO2 + 2СаО + С = Mn + 2CaO-SiO2 + СО — 178,8 кдж/моль (—42,69 ккал/моль).
При образовании жидких фаз активность закиси марганца в шлаках с высоким содержанием SiO2 остается пониженной, что затрудняет восстановление марганца в металлический раствор.
Поэтому благоприятные условия восстановления марганца создаются при значительном содержании в шлаке СаО. Эти условия достигаются раньше в случае применения офлюсованного агломерата с повышенной основностью. Закись марганца, будучи более слабым основанием, чем СаО, в присутствии последней имеет более высокую активность. Однако чрезмерное повышение основности шлака может привести к ухудшению условий восстановления марганца по, кинетическим причинам, из-за значительного повышения вязкости шлака. Условия восстановления марганца из расплава с высоким содержанием MnО при различной величине основности демонстрирует рис. 35. Повышение основности шлака до величины RO/SiO2 = 1,2 увеличивает степень восстановления MnО.
При низкой температуре (1360° С) наблюдается уменьшение степени восстановления при повышении основности.
В доменной печи восстановление MnО из жидкого шлака, вносящее основную долю марганца в чугун, протекает главным образом при температурах, начиная с 1200° С, т. е. в области нижней части распара, заплечиках и горне. Степень восстановления марганца составляет -~50%.
В связи со снижением необходимых содержаний марганца в чугунах для сталеплавильного производства при их выплавке в доменных печах нужны лишь минимальные добавки марганецсодержащих материалов. Кроме того, не требуется принятия специальных мер для возможно полного восстановления марганца шихты. Поэтому увеличивается производительность и снижается себестоимость продукта.
Обеспечение увеличения полноты восстановления марганца необходимо при плавке в доменной печи продуктов с повышенным его содержанием (зеркальный чугун и особенно ферромарганец). В этих случаях для максимального извлечения марганца из шихты и уменьшения его потерь необходимо иметь:
- повышенную основность шлака;
- снижение относительного количества шлака, что уменьшает абсолютные потери марганца;
- высокую температуру в нижних горизонтах печи.
Последнее достигается увеличением расхода кокса, максимальным нагревом дутья, и особенно эффективно, обогащением дутья кислородом. Так, выплавка ферромарганца на дутье, обогащенном кислородом до 30,7%, на Ново-Тульском металлургическом заводе позволила снизить расход кокса на 15—26% и повысить производительность в 1,5—2 раза по сравнению с работой на обычном дутье. Большую роль при этом играют уменьшение количества горнового газа, снижение температур отходящих газов и потерь тепла с ними.
Восстановление кремния
Значительные количества SiO2 содержатся в пустой породе руд, соединениях агломератов и в золе кокса. В составе агломератов кремний присутствует в виде силикатов железа, кальция и силикатов промежуточного состава (оливинов СаОx FeО(2-x) SiO2).
Двуокись кремния практически не восстанавливается газообразными восстановителями доменного газа СО и Н2, а может восстанавливаться только с участием углерода в области высоких температур. Выше 1500° С восстановление протекает с образованием значительных количеств легколетучего промежуточного окисла SiO, возгоны которого образуются при выплавке продуктов с повышенным содержанием кремния (ферросилиций и в меньшей степени литейные чугуны). При получении малокремнистых продуктов, в связи с более низкими температурами процесса, выделения SiO из зоны реакции практически не наблюдается.
Реакция восстановления SiO2 может быть записана следующим образом:
SiO2 + 2С = Si + 2СО — 611,27 кдж/моль (—146 ккал/моль).
Расчетная температура начала восстановления в стандартных условиях составляет 1540° С. Условия восстановления кремния из SiO2 значительно облегчаются при контактировании ее с железом. Восстанавливаемый кремний образует силициды железа, которые растворяются в железе и чугуне; в этом случае то же парциальное давление окиси углерода может достигаться при более низких температурах.

Лабораторными исследованиями было показано сильное возрастание степени восстановления SiO2 углеродом в присутствии металлического железа. Например, при 1300° С и выдержке в течение часа степень восстановления возрастала с 7 до 38 %.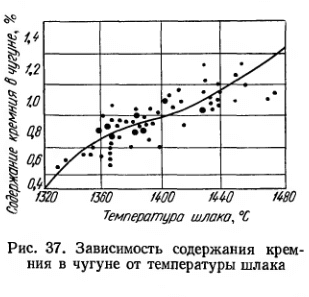
Однако в доменном процессе силикаты железа и марганца переходят в расплав еще до восстановления этих элементов. Более тугоплавкий силикат кальция CaO-SiO2 восстанавливается значительно труднее, чем свободная двуокись кремния (рис. 36). Восстановление кремния из твердой SiO2 и твердых силикатов не получает значительного развития, так как еще до этого эти вещества переходят в расплав — образующийся в доменной печи шлак. При восстановлении кремния из шлака условия процесса меняются. Активность SiO2 снижается вследствие уменьшения ее концентрации и растворения в шлаке основных окислов (FeO, MnО и особенно СаО).Легко восстановимые окислы шлака FeO и MnО дополнительно препятствуют восстановлению SiO2, восстанавливаясь в первую очередь. По данным производственных исследований, содержание кремния в металле на уровне распара намного ниже, чем у фурм и в конечном чугуне: 0,04—0,06 % Si в распаре и 1,3—1,5 % в выпускаемом чугуне; при выплавке ферросилиция в распаре содержится 2,5 % Si, на горизонте фурм 11,6 % Si.
Содержание кремния находится в тесной связи с температурой в горне, являясь надежным показателем его теплового режима (рис. 37). Для выплавки чугунов с более высоким содержанием кремния желательны трудноплавкие шлаки, повышающие температуру горна. Трудноплавкость шлака достигается обычно при повышенном содержании Аl2O3 в шихте.
При выплавке высококремнистых чугунов и ферросплавов сильно возрастает расход топлива. Для его снижения прибегают к повышению температуры дутья и обогащению его кислородом. В последнем случае получается более богатый продукт (18 % Si вместо 12 % Si без O2).
Восстановление фосфора
Основным источником фосфора в шихте являются руды или агломераты (в среднем 0,05—0,06% Р). В некоторых рудах содержание фосфора может доходить до 1,5%, и выплавляемые высокофосфористые чугуны требуют особой технологии их передела в сталь. Главные соединения фосфора в рудах и агломератах: Fe2O3•7Н2O, ЗFеО•Р2О5 и ЗСаО•Р2О5.
Фосфаты железа способны более легко восстанавливаться в силу своей меньшей химической прочности и облегчения восстановления фосфора контактированием с восстанавливаемым железом. Восстановление осуществляется окисью углерода и частично углеродом при 900—1100° С с образованием фосфида железа Fe2Р, растворяющегося в железе по реакциям:
2 (3Fе0·Р2O5) + 16СО = 3 [Fe2Р] + [Р] + 16СO2;
2 (3FeО·Р2О5) + 16С = 3 [Fe2Р] + [Р] + 16СО.
Преимущественно содержащееся в шихте соединение фосфора ЗСаO·Р2O5 является более химически прочным и интенсивно восстанавливается лишь при температурах с 1200° С с участием углерода:
ЗСаО·Р2О5 + 5С = ЗСаО + 2Р + 5СО — 1590 кдж/моль
(—379,65 ккал/моль).
Этот процесс также облегчается при контактировании с металлическим железом или чугуном, растворяющими фосфиды железа и фосфор. Ввиду позднего начала восстановления фосфора из фосфата кальция реакция не успевает закончиться до расплавления пустой породы и дальнейшее восстановление фосфора происходит из шлака. Несмотря на некоторое снижение активности фосфора в шлаке при повышении его основности фосфор практически полностью восстанавливается в чугун.
Таким образом, единственным средством получения чугуна с низким фосфором является подбор соответствующей шихты для доменного процесса.
Восстановление хрома, ванадия, никеля
При выплавке природнолегированных чугунов рудная часть шихты обычно содержит хром в виде хромита FeO (CaO, MgO) Сr2O3. Восстановление из него хрома происходит с участием углерода. В доменной печи хром полностью не восстанавливается в чугунки небольшая часть его теряется со шлаком. Степень восстановления составляет до 90%.
Окислы ванадия, присутствующие в некоторых фосфористых и титаномагнетитовых рудах, трудновосстановимы. Облегчающим условием является присутствие железа и повышенная основность шлака. Последняя увеличивает активность низших окислов ванадия в шлаке, имеющих слабоосновные свойства. Восстановление V2O3 и V2O2 происходит только при участии углерода, и при благоприятных условиях в чугун переходит 80% V шихты.
Закись никеля часто содержится в рудах вместе с соединениями хрома. Она восстанавливается гораздо легче FeO при небольших концентрациях СО в газе: NiO + СО = Ni + СO2. Температурный интервал протекания этой реакции в доменной печи 350— 900° С. В условиях доменной плавки извлечение никеля в чугун практически составляет 100%.