Металлы являются наиболее распространенным видом материалов, которыми человек удовлетворяет свои жизненные потребности. Сейчас человечество живет в век металлов и развитие всех отраслей промышленности, наука, культура и быт человека немыслимы без машин, механизмов, приборов и других изделий из металла.
Введение
Переход человека от использования камня (каменный век) к металлу был длительным и сложным. Он произошел не в результате революционного скачка в развитии общества, а металлы постепенно входили в обиход человека в течение длительного периода. Первым металлом, вошедшим в повседневный обиход человека, была медь, которая открыла эру металлургии и дала миру первый сплав – бронзу. По археологическим данным первые сведения о плавках меди относятся к 6500–5700 гг. до н.э. Она была основой материальной культуры в течение тысячелетий, и медный век постепенно перешел к бронзовому веку.
Следующим этапом в металлургии стало применение железа (железный век) и его начало относят ко второму тысячелетию до н.э. Получение чистого железа и его сплавов стало возможным благодаря накопленному опыту по выплавке меди, бронзы, золота и других легкоплавких металлов и сплавов. Освоение производства железа послужила мощным толчком к развитию производительных сил и технического прогресса. В древности человеку были известны восемь металлов – медь, золото, серебро, олово, свинец, железо, ртуть и сурьма. К концу XVIII в. их число увеличилось до 20, а в настоящее время производится и используется около 80 металлов.
Распространенность элементов в земной коре различна – от нескольких процентов до миллионных долей. Суммарное содержание десяти наиболее распространенных элементов (кислород – 47,00; кремний – 29,50; алюминий – 8,05; железо – 4,65, кальций – 2,96; натрий – 2,50; калий – 2,50; магний – 1,87; титан – 0,45; водород – 0,15) составляет 99,63 % массы земной коры, а на все остальные элементы приходится только 0,37 % общей массы земли. Представление о распространенности в земной коре некоторых хорошо известных металлов дают значения их кларков, т.е. среднеарифметическое содержание в земной коре, которые приведены ниже (%):

Наиболее редко в природе встречаются полоний и актиний, кларк которых близок к 10–15 %.
Техническое значение металла определяется его распространенностью в природе, потребностями в народном хозяйстве и производственными возможностями получения. Два последних фактора определяют масштабы производства отдельных видов металла. В производстве металлов около 95 % выпускаемой продукции (около 800 млн. т.) составляют чугун и сталь, которые представляют собой сплавы железа с углеродом и другими легирующими компонентами. Ежегодный выпуск основных цветных металлов находится на уровне (млн. т.): алюминий 23–24; медь 10–11; никель 0,5–0,7; свинец 4–5; цинк 5–6; магний 0,2–0,3; олово 0,20–0,25; молибден 0,14–0,15; титана около 0,1.
Производством металлов из руд и других видов металлосодержащего сырья занимается металлургия – крупнейшая отрасль тяжелой индустрии. Металлургия является центральным звеном горнометаллургического производства, включающего геологию, горное дело, обогащение, собственно металлургию, литейное производство и обработку металлов различными приемами (давлением, температурой, механическими методами и т.д.). В основе металлургии лежат принципы химических технологий, так как при осуществлении металлургических процессов перерабатываемые материалы претерпевают различные физико-химические превращения. Поэтому металлургия тесно связана с физикой, химией и особенно с физической химией, которая является научной основой теоретической и практической металлургии. В последние годы возрастает связь металлургии с математикой и компьютерной техникой.
Металлургическая промышленность России в настоящее время производит 78 элементов Периодической системы Д.И. Менделеева, а также различные виды удобрений, строительных материалов, серной кислоты и серы, цемента и многих других видов продукции. Металлургия России является высокоразвитой отраслью материального производства. Особое значение для развития горнозаводского дела в России имели труды M.B. Ломоносова, Д.И. Менделеева, а также крупных специалистов по производству черных металлов П.П. Аносова, Д.К. Чернова, Н.Н. Бекетова, И.П. Бардина и многих других. Неоценимый вклад в развитие отечественной цветной металлургии внесли А.А. Байков, НС. Курнаков, П.П. Федотьев, В.А. Ванюков, АИ. Беляев, И Ф. Худяков, АН Вольский и другие.
Металлы, их свойства и классификация
Большинство металлов обладает рядом свойств, имеющих общий характер и отличающихся от свойств других простых или сложных соединений. Такими свойствами являются сравнительно высокие температуры плавления большинства металлов, способность к отражению света, высокая теплопроводность и электропроводность, способностью к прокатыванию. Эти особенности объясняются существованием в металлах особого вида связи – металлической.
В соответствии с положением в периодической системе атомы металлов имеют небольшое число валентных электронов и много незаполненных орбит. Кроме того, валентные электроны достаточно слабо связаны со своими ядрами и поэтому обладают большой свободой перемещения в кристаллической решетке металла. общая картина металлического состояния может быть представлена в следующем виде. Узлы кристаллической решетки металла заняты как отдельными атомами, так и ионами, между которыми сравнительно свободно перемещаются электроны, называемые иногда электронным газом (рис.1).
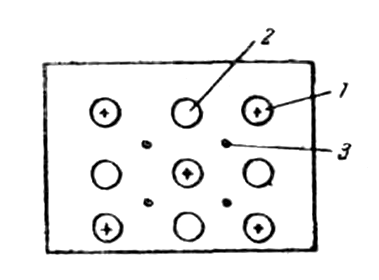
Поскольку валентные электроны распределены в кристалле металла почти равномерно, невозможно говорить о какой-либо направленности металлических связей. В этом состоит их важное отличие от ковалентных связей, которые имеют строгую направленность в пространстве. Металлическая связь отличается от ковалентной также и своей прочностью: ее энергия в 3–4 раза меньше энергии ковалентной связи. Существование подвижных электронов в кристалле металлов объясняет их характерные особенности (электропроводность, теплопроводность).
Металлическую связь можно определить как разновидность ненаправленной ковалентной химической связи, когда атомы имеют мало валентных электронов, много свободных орбит, а валентные электроны слабо удерживаются ядром
Таким образом, металлы – химические элементы, кристаллические решетки которых состоят из атомов и ионов, а в пространстве между ядрами свободно перемещаются электроны. Связь между атомами ковалентная, между ионами и электронами – металлическая.
Атомы постоянно теряют электроны, превращаясь в ионы, а последние принимают их, становясь атомами. Количество электронов, беспорядочно блуждающих в кристаллической решетке, подобно молекулам газа, у разных металлов различно, оно определяет долю металлической связи и меру металличности элемента.
Представление о кристаллической решетке – «погруженной в облако свободно блуждающих электронов», – впервые высказанное в 1902 г., теперь дополнено и приобрело несколько измененную трактовку; однако оно и в первоначальном упрощенном виде хорошо объясняет высокую электропроводность, теплопроводность и термоэлектронную эмиссию металлов.
На атомы и ионы в узлах кристаллической решетки действуют силы взаимного притяжения и отталкивания. Амплитуды колебания ионов и атомов зависят от температуры и возрастают с ней. При температуре плавления амплитуды колебаний столь велики, что решетка разрушается: атомы и ионы теряют свои постоянные места и переходят в беспорядочное движение, свойственное жидкому состоянию. Связь между ионами и электронами называют металлической, а между атомами – ковалентной. От соотношения этих видов химической связи зависит количество блуждающих электронов. Чем больше это количество, тем ярче выражены металлические свойства элементов.
Прочностью металлической связи объясняются многие физические и механические свойства металлов.
Внешние механические воздействия на металл вызывают сдвиг слоев кристаллической решетки, однако связь между ионами и электронами при этом не нарушается из-за свободной подвижности электронов. По этой причине металлы прочны и пластичны, они изменяют форму, но не теряют прочности. В меди и золоте много свободных электронов, металлическая связь значительно преобладает над ковалентной – эти металлы пластичны, ковки, вязки. У сурьмы и висмута свободных электронов сравнительно мало, поэтому они хрупки.
Некоторые физические и механические свойства наиболее распространенных цветных металлов приведены (таб.1).
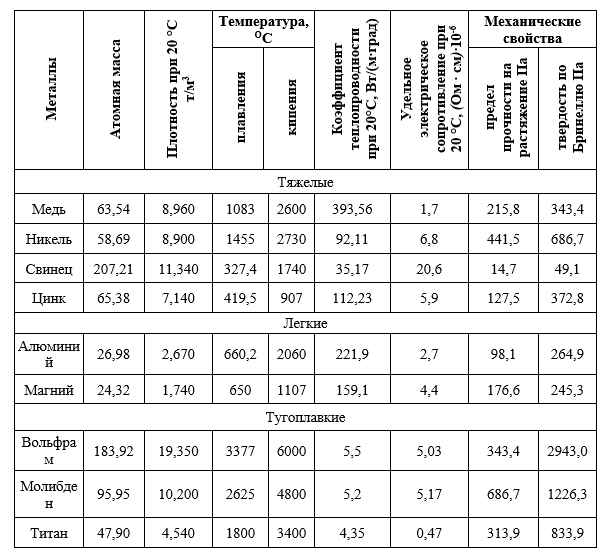
Физические и механические свойства наиболее распространенных, цветных металлов
Электропроводность, обусловленная перемещением в пространстве кристаллической решетки «обобществленных» электронов, очевидно, зависит от свободы их передвижения – правильности расположения атомов, амплитуды и частоты их теплового колебания. Действительно, с повышением температуры размах колебания узлов решетки увеличивается, рассеивание электронов усиливается, и электропроводность снижается; с охлаждением она снова возрастает. При температурах, близких к абсолютному нулю, электрическое сопротивление некоторых металлов и сплавов становится исчезающе малым. Необходимость очень низких температур пока затрудняет практическое использование этого ценного и интересного явления. Сверхпроводимость при минус 253 °С, обнаруженная в середине XX века у сплава ниобия, алюминия и германия, – редкое явление. Другой такой «высокотемпературный» сверхпроводник представляет собой сплав из ниобия и галлия.
Присутствие даже малых примесей других элементов понижает электропроводность: нарушая порядок в решетке, они рассеивают электроны. Также рассеивают электроны атомы, перемещенные в результате внешнего механического воздействия, – деформации ковкой, прокаткой или иной подобной обработкой.
Теплопроводность почти всегда изменяется с температурой подобно электропроводности – наиболее электропроводные металлы хорошо проводят тепло, а имеющие сравнительно высокое электрическое сопротивление – хуже. Теплопроводность связана как с колебаниями атомов в решетке, так и с движением свободных электронов. Последнее, по-видимому, имеет преобладающее значение.
Механические свойства – прочность на разрыв, сжатие, изгиб, твердость и пластичность объясняются не только металлической связью, но и особенностями кристаллической структуры металлов, имеющей в большинстве плотноупакованные пространственные решетки с высоким координатным числом. Наиболее типичные из них показаны (рис. 2), который надо понимать только как схему расположения атомных центров. В действительности, атомы, условно представляемые в виде шаров, плотно упакованы и занимают только 70 % объема (см. рис.2 г, 1).
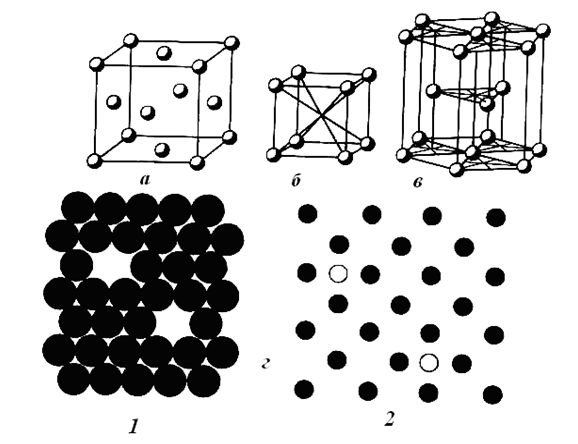
а – кубическая гранецентрированная решетка меди (аналогичны Аи, Ag, Al, Pt и др.); б – кубическая объемно-центрированная решетка вольфрама (аналогичны Fe, К. Ва и др.); в – гексагональная плотная решетка магния (аналогичны Zn, Be и др.); г – дефекты структуры: 1 – вакансии; 2 – междоузлия, включающие примесь
Многие металлы взаимно растворимы в жидком или твердом состояниях, либо образуют между собой химические – интерметаллические соединения, вследствие этого возникают иные кристаллические системы и широко изменяются свойства. Речь идет о сплавах, которые открывают простор получению новых ценных материалов с особыми свойствами. Уже применяют тысячи двойных, тройных и более сложных сплавов, которые получают не только смешиванием жидких металлов, но и спеканием порошков или растворением какого-либо элемента в поверхностном слое твердого металла (сплава).
Способность к упругим и пластическим деформациям, высокие электропроводность и теплопроводность, и некоторые другие особенности составляют комплекс свойств, не присущий иным твердым телам – дереву, камню, пластмассам. Этим и объясняется неоспоримое признание металлов и сплавов важнейшими материалами современной техники.
М. В. Ломоносов определял металлы как «…светлые тела, которые ковать можно». В наши дни, помимо дополнения этого признаками высокой электропроводности и теплопроводности, надо отметить и зависимость многих свойств от чистоты и механической обработки. Один и тот же металл может быть и ковким и хрупким. В реальных кристаллах всегда есть различные дефекты, из-за которых механические и другие физические свойства нельзя отнести только к особенностям металлической связи и кристаллической решетки.
Точечные дефекты – незаполненные узлы решетки, вакансии (см. рис. 2), а также узлы, занятые атомами примесей, возникают при кристаллизации из расплава. Линейные и плоские дефекты – дислокации получаются также при кристаллизации либо в результате механической обработки в виде неполных слоев атомов или их взаимного смещения, а иногда и переплетения.
Общее количество дефектов на 1 см2 площади металла или сплава часто превышает 106. Точечные дефекты снижают преимущественно электропроводность и теплопроводность, а другие – еще и механические свойства.
Обычные металлы и сплавы поликристалличны, они состоят из произвольно ориентированных совокупностей зерен. в каждом зерне элементарные кристаллы имеют одинаковую ориентацию, а в соседних – отличную, иногда расположенную под большими углами (рис. 3). На границах зерен скапливаются примеси и образуются газовые пустоты. Помимо понижения физических свойств, здесь наблюдается и меньшая коррозионная стойкость.
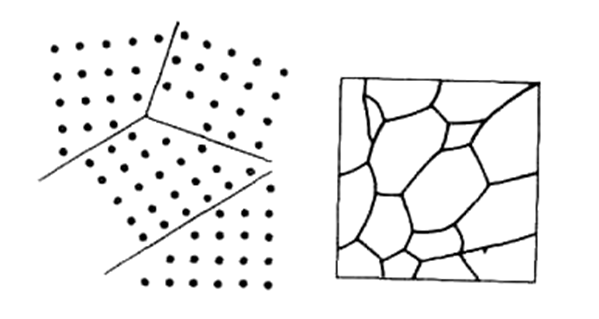
Возможность смещения слоев кристаллов по направлениям дислокаций или разрыв их на границах зерен понижают прочность. Прочность в известной мере возрастает после отжига – нагревания и медленного охлаждения, когда в результате диффузии дислокации частично устраняются, а зерна становятся мельче.
Механическая обработка иногда вызывает упрочнение, связанное с переплетением дислокаций. Другая причина существенного упрочнения, сопровождающегося понижением пластичности и появлением хрупкости, связана с возникновением или введением посторонних нерастворимых фаз, например, карбида железа F3C в стали или окислов и нитридов в титане, вольфраме, молибдене. Зерна этих соединений препятствуют взаимному смещению слоев металла. Очистка металлов от примесей обычно значительно улучшает ковкость и облегчает обработку.
Жидкие металлы отличаются от твердых металлов сравнительно малой связью между атомами и ионами, но свобода движения электронов и здесь сохранена, поэтому они также электропроводны и теплопроводны.
Один и тот же металл при разных температурах может иметь разные кристаллические решетки. Переход из одной системы в другую изменяет расстояние между узлами и их расположение, этот переход существенно отражается на свойствах полиморфных модификаций. Например, олово, известное при обычных температурах как пластичный блестящий металл тетрагональной сингонии с плотностью 7,29 г/см3 (β – модификация), при температурах ниже 13,2 °С, а особенно при быстром переохлаждении превращается в серый порошок, кристаллизуясь в кубической системе с плотностью 5,85 г/см3 (α – модификация). Подобные превращения свойственны многим другим элементам.
Химическую активность металлов можно характеризовать положением в электрохимическом ряду напряжений, где металлы размещены в порядке нарастания нормальных электрохимических или электродных потенциалов. Чем больше алгебраическая величина нормального электродного потенциала, тем меньше восстановительная способность и химическая активность металла. В ряду напряжений каждый металл способен вытеснять стоящие правее него металлы из водных растворов и солевых расплавов.
Металлы с отрицательными электрохимическими потенциалами легко подвержены окислению, поэтому они встречаются в природе только в виде химических соединений: оксидов, галогенидов, а также сульфидов, силикатов и других солей. По мере повышения потенциала, а значит и снижения химической активности, свободное состояние металлов становится все более устойчивым. Например, медь, серебро и ртуть находятся в природе не только в виде солей, но и в свободном состоянии, а золото и платина – преимущественно в свободном состоянии. Связь между электродными потенциалами и некоторыми свойствами металлов показана (табл. 2).
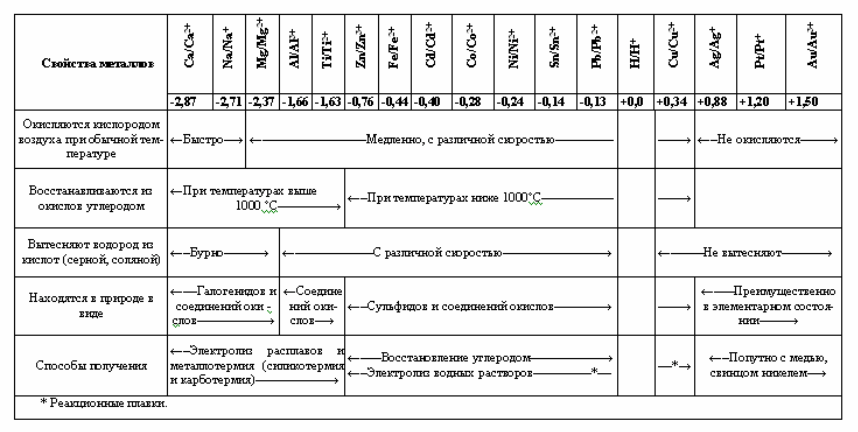
Характеризуя металлы как химические элементы надо заметить, что Периодическая система Д. И. Менделеева не позволяет четко различить их от металлоидов и неметаллов. Это и естественно: каждый элемент представляет собой диаэлектрическое единство металлических и металлоидных свойств, противоречивая природа которых не устраняется с ростом заряда ядра и количества электронных оболочек.
Явными неметаллами легко признать водород, благородные газы, галогены, элементы группы VI – кислород, серу, селен, теллур и полоний, а также бор, углерод, азот, кремний и фосфор. Все они не дают основных оксидов и гидрооксидов, свойственных металлам. Вместе с тем из числа прочих элементов некоторые имеют амфотерные гидрооксиды. В частности, у таких, казалось бы, явных металлов, как цинк и алюминий, оксиды проявляют и кислотные и основные свойства.
О кристаллических решетках металлов в общем случае говорилось выше, а для большинства химических элементов они условно показаны в табл. 4. Однако различие кристаллических структур также не дает оснований для интересующего нас подразделения элементов. Привычно считаемые металлами ртуть, и висмут кристаллизуются в несвойственной большинству других металлов ромбической системе, а индий и олово – в тетрагональной.
Наиболее четкую условную границу между металлами и металлоидами можно провести, сравнивая электропроводность или обратную ей величину – удельное электрическое сопротивление. Для явного металла – никеля удельное электрическое сопротивление равно 6,8∙10–6 (Ом∙см), а для металлоида углерода только в модификации графита составляет 1375∙10–6 (Ом∙см).
Ориентируясь по этому признаку, к металлам следует отнести 80 элементов, а к неметаллам и металлоидам 23.
Далее, ограничивая область металлургии элементами, входящими в состав земной коры, из восьмидесяти следует исключить франций, технеций, прометий, а также актиниды, начиная с америция, и определить окончательное число металлов, равным 68 (таб. 3).
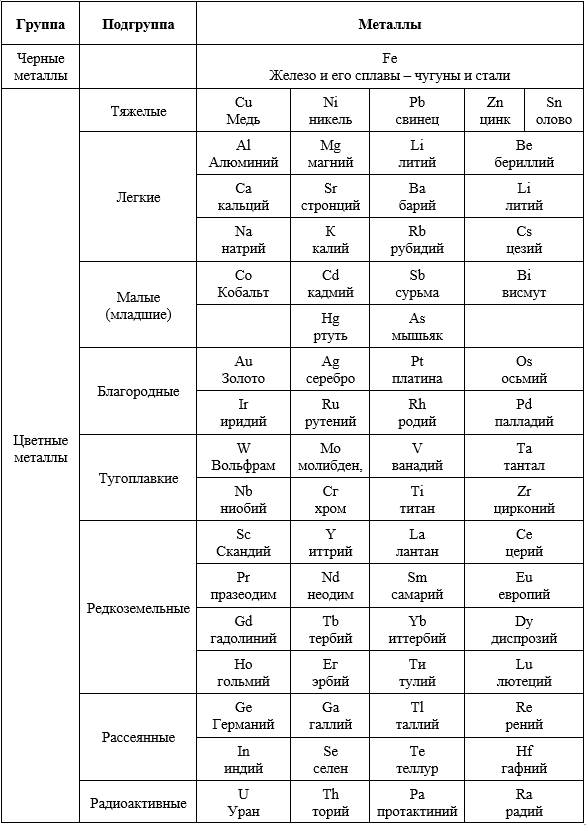
Промышленная классификация металлов
в связи со стремлением к комплексности использования сырья, а также широким производством сплавов, часто включающих металлоиды, сложились традиции, по которым к металлам иногда неправильно относят кремний, германий, а иногда также селен и теллур, попутно извлекаемые из металлургического сырья. Наряду с этим типичный металл – натрий получает химическая промышленность; из этого видна тесная связь химии с металлургией. Раньше металлургию отличало от химической технологии преимущественное применение плавок при высоких температурах, теперь эта особенность все более утрачивается: наряду с огневой пирометаллургией возрастает значение гидрометаллургии, которая извлекает металлы из руд выщелачиванием водными растворами реагентов с последующим восстановлением электролизом либо цементацией.
В качестве промежуточных переделов для разделения и концентрирования растворенных веществ пользуются сорбцией, экстракцией, осаждением, соосаждением и другими способами химической переработки.
Промышленная классификация металлов, традиционно сложившаяся в нашей стране в период наиболее интенсивной индустриализации, не имеет четкой научной основы, но широко применяется в технической литературе и обиходе. Первое основание ее, принятое и в некоторых других странах, состоит в резком различии масштабов производства железа и прочих металлов. В общей массе металлургической продукции, сплавы железа занимают около 93%. Поэтому различают «железные металлы» (железо и его сплавы – чугуны и стали) и прочие «нежелезные».
У нас этому соответствуют условно принятые названия черные и цветные металлы. Цветные металлы в свою очередь подразделяются по некоторым общим признакам на ряд групп и подгрупп, отмеченных в табл.3 и 4.

В вышеприведенной классификации нет даже принципа названий групп. Так, в конце прошлого столетия алюминий считали редким металлом, а сейчас по производству и потреблению он занимает первое место среди цветных металлов. Не решен окончательно вопрос и с титаном, так как некоторые металлурги относят его к тугоплавким редким металлам, а другие к легким металлам. Поэтому различные металлурги, придерживаясь разных точек зрения, относят отдельные металлы к разным группам.